Лактоза , или молочный сахар , содержится только в молоке и служит важным источником энергии для детенышей млекопитающих. Она переваривается медленно и потому способна обеспечивать постоянный стабильный приток энергии.
Сахароза , или тростниковый сахар - самый распространенный в природе полисахарид. Чаще всего она встречается в растениях, где в больших количествах транспортируется по флоэме. Сахароза особенно пригодна для этого, так как благодаря ее высокой растворимости она может транспортироваться в виде весьма концентрированных растворов.
В химическом отношении сахароза довольно инертна, т. е. при перемещении из одного места в другое она практически не вовлекается в метаболизм. По этой же причине сахароза иногда откладывается в качестве запасного питательного вещества. Промышленным способом сахарозу получают из сахарного тростника или сахарной свеклы; именно она и есть тот самый «сахар»,который мы обычно покупаем в магазине.
Редуцирующие сахара
Все моносахариды и некоторые дисахариды, в том числе мальтоза и лактоза, относятся к группе редуцирующих (восстанавливающих).
Сахаров , т. е. соединений, способных вступать в реакцию восстановления. представляет собой единственный нередуцирующий сахар среди распространенных Сахаров. Две обычные реакции на редуцирующие сахара - реакция Бенедикта и реакция Фелинга - основаны на способности этих Сахаров восстанавливать ион двухвалентной меди до одновалентной. В обеих реакциях используется щелочной раствор сульфата меди(II) (CuSO 4), который восстанавливается до нерастворимого оксида меди(1) (Cu 2 0).

Введение
Йодометрией называют метод объемного анализа, в ос-нове которого лежат реакции:
Методом йодиметрии можно определять как окисли-тели, так и восстановители.
Определение окислителей. Методом йодиметрии можно определять те окислители, которые количественно окисляют IЇ в свободный I2. Чаще всего определяют перманганаты, бихроматы, соли меди (II), соли желе-за (III), свободные галогены и др. Индикатором в методе йодиметрии служит раствор крахмала. Это чувствительный и специфический инди-катор, образующий с йодом адсорбционное соединение синего цвета.
Определение восстановителей. Из числа восстано-вителей этим методом чаще всего определяют сульфиты, сульфиды, хлорид олова (II) и др. Рабочим раствором является раствор йода I2. Метод йодиметрии широко применяется в химическом анализе. Этим методом определяют соединения мышьяка (III); медь (II) в солях, рудах; многие органические лекарственные препараты - формалин, анальгин, аскорбиновую кислоту и др.Цель работы: определение редуцирующих сахаров в различных кондитерских изделиях.
Отработка методики количественного определения редуцирующих сахаров в рабочем растворе.
Установить соответствие нормальным содержаниям редуцирующих сахаров в кондитерских изделиях содержащихся в ГОСТ
Основным сырьем для производства кондитерских товаров служат сахар, инвертный сироп, мука, жиры, молоко. Кроме того, при производстве кондитерских изделий используются фрукты и ягоды, орехи, какао-бобы, мед, пряности также многие другие продукты.
В формировании потребительских свойств кондитерских изделий большая роль придается продуктам, которые придают им структуру, внешний вид, вкус и цвет: студнеобразователям, эмульгаторам, пенообразователям, красителям, ароматизаторам.
редуцирующий сахар кондитерский потребительский
Сахар. Редуцирующие сахара
Продукт представляет собой чистый углевод - сахарозу, характеризуется приятным сладким вкусом и высокой усвояемостью. Обладает большой физиологической ценностью, возбуждающе действует на ЦНС, способствуя обострению органов зрения, слуха; является питательным веществом для серого вещества мозга; участвует в образовании жира, белково-углеводных соединений и гликогена. При избыточном употреблении сахара развиваются ожирение, сахарный диабет, кариес. Суточная норма - 100 г, в год - 36,5 кг, но ее следует дифференцировать в зависимости от возраста и образа жизни.
Инвертный сироп
Инвертный сироп служит заменителем патоки, так как обладает антикристаллизационными свойствами. Получают инвертный сироп нагреванием водного раствора сахара с кислотой, при этом происходит процесс инверсии, заключающийся в расщеплении сахарозы на фруктозу и глюкозу. Для инверсии используются кислоты: соляная, лимонная, молочная, уксусная.
Редуцирующий сахар
Все моносахариды, в случае с сиропом глюкоза и фруктоза, и некоторые дисахариды, в том числе мальтоза и лактоза, относятся к группе редуцирующих (восстанавливающих) сахаров, т. е. соединений, способных вступать в реакцию восстановления.
Две обычные реакции на редуцирующие сахара -- реакция Бенедикта и реакция Фелинга -- основаны на способности этих сахаров восстанавливать ион двухвалентной меди до одновалентной. В обеих реакциях используется щелочной раствор сульфата меди(II) (CuSO4), который восстанавливается до нерастворимого оксида меди(1) (Cu2O).
Реакция Фелинга наиболее часто используется для доказательства восстанавливающих свойств сахаров, она заключается в восстановлении моносахаридами гидроксида меди (II) в закись меди (I). При проведении реакции используется реактив Фелинга, представляющий собой смесь сульфата меди с сегнетовой солью (калий, натрий виннокислый) в щелочной среде. При смешивании сульфата меди со щелочью образуется гидроксид меди.
CuSO4 + 2NaOH -> Cu(OH)2v + Na2SO4
В присутствии сегнетовой соли выделившийся гидроксид не выпадает осадок, а образует растворимое комплексное соединение меди (II), которое восстанавливается в присутствии моносахаридов с образованием закисной меди (I). При этом альдегидная или кетон- группа моносахарида окисляется до карбоксильной группы. Например, реакция глюкозы с реактивом Фелинга.
СН2ОН - (СНОН) 4 - СОН + Сu(ОН) 2 ===> СН2ОН - (СНОН) 4 - СООН + Сu2Оv+ Н2О
Значение сахаров для организма
Фруктоза.
Фруктоза менее распространена, чем глюкоза, и также быстро окисляется. Часть фруктозы в печени превращается в глюкозу, но для своего усвоения она не требует инсулина. Этим обстоятельством, а также значительно более медленным всасыванием фруктозы сравнительно с глюкозой в кишечнике, объясняется лучшая переносимость ее больными сахарным диабетом.

Глюкоза - составная единица, из которой построены все важнейшие полисахариды - гликоген, крахмал, целлюлоза. Она входит в состав сахарозы, лактозы, мальтозы. Глюкоза быстро всасывается в кровь из желудочно-кишечного тракта, затем поступает в клетки органов, где вовлекается в процессы биологического окисления. Метаболизм глюкозы сопровождается образованием значительных количеств аденозинтрифосфорной кислоты (АТФ), являющейся источником уникального вида энергии. АТФ во всех живых организмах играет роль универсального аккумулятора и переносчика энергии. В медицине препараты аденозина применяют при спазмах сосудов и мышечной дистрофии, и это доказывает важность для организма АТФ и глюкозы.
Во время бодрствования организма энергия глюкозы восполняет почти половину его энергетических затрат. Оставшаяся невостребованной часть глюкозы преобразуется в гликоген - полисахарид, который хранится в печени.
Методы определения сахара в кондитерских изделиях
Поскольку контроль содержания уровня сахара в организме необходим, существует целый ряд различных методов определения количества как общих, так и редуцирующих (инверсных) сахаров в кондитерских изделиях,что является важной частью контроля качества производства данной продукции.
Иодиметрический метод
Метод основан на восстановлении щелочного раствора меди некоторым количеством раствора редуцирующих сахаров и определении количества образовавшегося оксида меди (1) или невосстановившейся меди йодометрическим способом.
Метод применяется для всех видов кондитерских изделий и полуфабрикатов, кроме мучных кондитерских изделий, полуфабрикатов для тортов и пирожных и восточных сладостей.
Метод применяется при возникновении разногласий в оценке качества.
Перманганатный метод
Метод основан на восстановлении соли железа (III) оксидом меди (I) и последующем титрова-нии восстановленного оксида железа (И) перманганатом.
Поляриметрический метод
Метод основан на измерении вращения плоскости поляризации света оптически активными ве-ществами.
Метод применяется для определения массовой доли общего сахара в шоколаде, пралине, какао- напитках, шоколадных пастах, сладких плитках, шоколадных полуфабрикатах без добавлений и с добавлением молока.
Восстановительный сахар является химическим термином для сахара, который действует как восстановитель и может пожертвовать электроны другой молекуле. В частности, восстанавливающий сахар является типом углеводов или натурального сахара, который содержит свободную альдегидную или кетоновую группу. Сокращение сахара может вступать в реакцию с другими частями пищи, такими как аминокислоты, для изменения цвета или вкуса пищи.
Видео дня
Различные типы сахара
Сахара встречаются естественным образом во всех фруктах, овощах, молочных продуктах и цельных зернах. Эти природные сахара иначе известны как углеводы, существенные макроэлементы. Диетические углеводы классифицируются как моносахариды, которые являются молекулами одного сахара; дисахариды - две молекулы сахара связаны между собой; или олигосахариды и полисахариды, которые являются более длинными цепями молекул сахара. Моносахариды включают глюкозу, галактозу и фруктозу, которые все уменьшают сахара. Моносахариды нередко встречаются в природе по отдельности, но они являются компонентами дисахаридов и полисахаридов. По этой причине некоторые дисахариды, такие как мальтоза, также уменьшают сахара.
Примеры редуцирующих сахаров
Самым важным моносахаридом и восстановительным сахаром является глюкоза. В организме глюкоза известна как сахар крови, потому что она необходима для функции мозга и физической энергии. Фруктоза - еще один восстановительный сахар и известен как самый сладкий из всех моносахаридов. Галактоза, еще один восстановительный сахар, является компонентом лактозы, которая содержится в молочных продуктах. Мальтоза не часто встречается в природе, но она образуется во время пищеварения, когда молекулы крахмала разрушаются.
Реакция Майара
Реакция Майара представляет собой процесс, который возникает, когда восстанавливающий сахар реагирует с амином, что приводит к поджариванию пищи. Эта реакция обычно возникает, когда пища нагревается или остается при комнатной температуре в течение длительного периода времени. Процесс поджаривания проявляется на коре хлеба или на коже обжаренной индейки. Реакция Майара также способствует вкусу и аромату многих продуктов питания, таких как кофе, шоколад и печеный хлеб.
Невосстанавливающие сахара
Некоторые дисахариды, такие как сахароза, являются нередуцирующими сахарами, то есть они не могут пожертвовать электроны другим молекулам. Сахароза состоит из двух восстанавливающих сахаров, глюкозы и фруктозы и не содержит свободных карбонильных групп. Сахароза встречается естественным образом во многих пищевых продуктах и часто добавляется во многие обработанные пищевые продукты, чтобы способствовать сладости.
Общие сведения.
Фруктоза, окисляясь, образует одноосновную арабоновую кислоту и формальдегид, которые при дальнейшем окислении дают соответственно триоксиглутаровую и муравьиную кислоты. При взаимодействии реактива Фелинга с редуцирующими сахарами (при нагревании) происходит разложение медного алкоголята сегнетовой соли:

Освобождающаяся окись меди быстро восстанавливается в закись
Выделяющийся при этой реакции кислород окисляет сахара. Следовательно, по количеству образовавшейся закиси меди можно рассчитать содержание редуцирующих сахаров в исследуемом материале.
Реактивы: а) реактив Фелинга (приготовление см. с. 202). 1 мл реактива должен соответствовать 0,05 г инвертного сахара (смеси равных количеств глюкозы и фруктозы). Методика установки титра реактива Фелинга описана ниже (см. с. 224); б) метиленовая синь (метиленовая голубая), 1%-ный раствор; в) натрий углекислый, 15%-ный раствор; г) уксуснокислый свинец раствор; д) фосфорнокислый натрий двузамещенный - , насыщенный раствор; е) соляная кислота, концентрированная едкий натр, раствор.
Приготовление вытяжки.
Из средней пробы продукта берут навеску, величина которой зависит от предполагаемого содержания сахаров в материале. При исследовании фруктов или ягод навеска составляет 15-50 г мезги (материала, измельченного на терке или мясорубке), варенья, повидла, джема - 7-8 г. Навеску количественно переносят в мерную колбу на 250 мл, смывая ее дистиллированной водой. Объем навески и воды в колбе не должен превышать 130-150 мл. Колбу встряхивают, затем определяют реакцию содержимого (с помощью нейтральной лакмусовой бумаги или универсального индикатора). При исследовании фруктов и ягод реакция вытяжки обычно бывает кислой, поэтому ее доводят до нейтральной (pH 7) осторожным добавлением 15%-ного раствора углекислого натрия (под контролем лакмуса или универсального индикатора), после чего колбу нагревают в течение 15-20 мин. на горячей водяной бане (80°С), часто встряхивая для перемешивания содержимого.
Примечание. При исследовании продуктов, содержащих крахмал (например, клубней картофеля, незрелых яблок и груш), водную вытяжку не нагревают на водяной бане, а сахара извлекают холодной водой в течение 1 ч, часто взбалтывая колбу.
Колбу охлаждают и к вытяжке добавляют 7-15 мл раствора уксуснокислого свинца, взбалтывают и ставят на 5-10 мин. (для осаждения белков, пигментов, дубильных веществ, также обладающих восстанавливающими свойствами). Появление прозрачного слоя жидкости над осадком свидетельствует о полноте осаждения. Если полнота
осаждения не была достигнута, в колбу добавляют (каплями) еще 1-5 мл раствора уксуснокислого свинца и взбалтывают. Для осаждения избытка уксуснокислого свинца в колбу приливают 18-20 мл насыщенного раствора двузамещенного фосфорнокислого натрия, взбалтывают и оставляют на 10-12 мин. для отстаивания. Проверяют полноту осаждения свинца, для чего по стенке колбы осторожно приливают 1-2 капли раствора фосфорнокислого натрия. Если в прозрачном слое жидкости над осадком уже не образуется мути, считают, что полнота осаждения достигнута. Колбу доливают до метки водой, взбалтывают и содержимое ее фильтруют через бумажный складчатый фильтр. В фильтрате (его называют «фильтрат А») определяют содержание редуцирующих сахаров. Надо так подобрать навеску продукта и разведение, чтобы концентрация сахаров в фильтрате А составляла .
Примечание. Быстрого осаждения белковых, красящих и дубильных веществ (так называемых органических несахаров) можно достигнуть обработкой вытяжки основным азотнокислым свинцом. К 100 мл вытяжки прибавляют 3-4 мл раствора едкого натра, взбалтывают и добавляют 4-6 мл раствора азотнокислого свинца. Осветление раствора происходит в течение 5-7 мин. Для освобождения от избытка свинца к вытяжке, нагретой до температуры 60° С, приливают 3-4 мл насыщенного раствора сернокислого натрия и нагревают на водяной бане при той же температуре 10 мин.
Определение редуцирующих сахаров (по Лэну и Эйнону).
В фильтрате А содержатся редуцирующие сахара (глюкоза, фруктоза и другие монозы, а также дисахариды, обладающие восстанавливающими свойствами, - мальтоза, лактоза и др.). Хотя сахароза тоже переходит в фильтрат, но для количественного определения ее необходимо подвергнуть гидролитическому расщеплению, инверсии (см. с. 222).
Метод определения редуцирующих сахаров основан на титровании реактива Фелинга сахарным раствором (фильтратом А) в присутствии метиленовой сини. Сахара, оставшиеся в небольшом избытке после восстановления окиси меди в закись, реагируют с метиленовой синью, восстанавливая ее в лейкосоединение.
В бюретку емкостью 50 мл (со стеклянным краном) наливают фильтрат А. В коническую колбу специальными
пипетками вносят по 5 мл растворов Фелинга I и II и вливают из бюретки 15-20 мл фильтрата А. Колбу ставят на электрическую плитку и нагревают (на асбестовой сетке) так, чтобы довести до кипения за 2 мин., после чего прибавляют 4-5 капель раствора метиленовой сини и кипятят точно 2 мин.
Примечание. Могут наблюдаться случаи, когда от прибавления метиленовой сини раствор в колбе не посинеет. Это свидетельствует о высокой концентрации редуцирующих сахаров в фильтрате А, и тогда надо его разбавить в два-три раза. Содержание сахаров в испытуемом растворе должно составлять примерно
Продолжая кипячение жидкости, ее титруют из бюретки фильтратом А до исчезновения синего окрашивания и появления оранжевого осадка закиси меди.
Титровать надо быстро, чтобы в сумме жидкость кипела не более 3 мин. На дотитровывание следует расходовать не более 2-3 мл испытуемого раствора. Если при этом расходуется более 3 мл фильтрата А, рекомендуется повторить определение, прибавив в колбу не 15, а 20 мл испытуемого раствора.
Первое титрование является ориентировочным. Приблизительно установив, сколько миллилитров фильтрата А расходуется на титрование 10 мл реактива Фелинга, проводят два-три точных определения.
где Т - титр реактива Фелинга (по инвертному сахару); н - навеска растительного материала в объеме испытуемого раствора, израсходованном на титрование 10 мл реактива Фелинга (суммируют количество миллилитров фильтрата А, прибавленных в колбу в самом начале определения и затем затраченных на дотитровывание)
Определение сахарозы.
Для определения содержания сахарозы в отдельной порции фильтрата А производят ее гидролитическое расщепление (инверсию). Условия инверсии подобраны так, что гидролизуется только одна сахароза.

В мерную колбу на 100 мл вносят 50 мл фильтрата А (см. с. 221), добавляют 5 мл концентрированной соляной кислоты и нагревают, часто взбалтывая, в течение 8 мин. на водяной бане, следя за тем, чтобы жидкость в колбе имела температуру 68-70° С (шарик термометра опущен в колбу). Затем колбу быстро охлаждают (под краном) до 20° С. Охлажденную жидкость нейтрализуют углекислым натрием или раствором едкого натра, контролируя этот процесс лакмусовой бумажкой, опущенной в колбу. Нейтрализованную жидкость доводят водой до метки и в случае необходимости фильтруют. Получают фильтрат Б, в котором содержится так называемый инвертный сахар - смесь равных частей глюкозы и фруктозы, освободившихся в результате гидролитического расщепления сахарозы. Содержание редуцирующих сахаров в фильтрате определяют по методу, описанному выше.
где - содержание соответственно редуцирующих сахаров и сахарозы.
Определение титра реактива Фелинга.
Титр реактива Фелинга определяют по химически чистой сахарозе.
Примечание. Для установки титра реактива можно также пользоваться сахаром-рафинадом, который предварительно выдерживают в эксикаторе (над хлористым кальцием) в течение 4-б суток.
На аналитических весах (с точностью до 0,0001 г) отвешивают 0,55 г сахарозы. Навеску переносят в мерную колбу на 250 мл и растворяют в 75 мл теплой воды.
К раствору прибавляют 4 мл концентрированной соляной кислоты и производят инверсию сахарозы. Все последующие операции описаны выше (см. «Определение сахарозы»). Определяют содержание редуцирующих сахаров в растворе.
Пример расчета. Навеска сахарозы - 0,55 г. Объем растворта инвертного сахара - 250 мл. На титрование 10 мл реактива Фелинга израсходовано 21,2 мл испытуемого раствора.
Титр реактива Фелинга (по инвертному сахару) рассчитывают по формуле
![]()
где н - навеска сахарозы, г, В - объем раствора инвертного сахара, израсходованный на титрование 10 мл реактива Фелинга (в нашем примере - 21,2 мл); а - объем раствора инвертного сахара в мерной колбе ( - коэффициент перевода сахарозы в инвертный сахар;

Изобретение относится к определению редуцирующих веществ и может быть использовано в кондитерском, карамельном и сахаропаточном производстве. Способ включает окисление редуцирующих веществ соединениями меди (II) в щелочной среде при нагревании на кипящей водяной бане в течение 10 минут, доведение объема охлажденного раствора до определенного значения, определение оптической плотности при длине волны 670 нм, введение поправки на частичное окисление нередуцирующих углеводов, которую вычитают из показания оптической плотности, и оценку концентрации редуцирующих веществ по калибровочному графику. Достигается повышение точности и воспроизводимости анализа. 5 пр., 6 табл., 4 ил.
Изобретение относится к способу определения редуцирующих веществ и может быть использовано в кондитерском, карамельном и сахаропаточном производстве.
Содержание редуцирующих веществ в карамели строго регламентировано и составляет не более 20% для неподкисленной карамели, не более 23% для карамели с введением кислоты свыше 0,6% и не более 32% для изделий с лактозой [ГОСТ 6477-88 Карамель. Общие технические условия.]. Избыток редуцирующих сахаров может привести к адсорбции влаги из воздуха и отсыреванию продукта. Недостаток редуцирующих веществ вызывает кристаллизацию сахарозы внутри изделия, что сказывается на его качестве при длительном хранении.
По количеству редуцирующих веществ судят о степени гидролиза крахмала в сахаропаточном производстве, именно этот показатель главным образом определяет вид продукта: для патоки низкоосахаренной содержание редуцирующих веществ составляет 26-35%, для карамельной кислотной и карамельной ферментативной - 36-44%, для мальтозной - 38% и более, для высокоосахаренной - 45% и более [ГОСТ Р 52060-2003 Патока крахмальная. Общие технические условия].
Известны способы, основанные на определении содержания редуцирующих веществ, основанные на титриметрическом определении оксида меди (I), выделяющегося в результате восстановления двухвалентной меди редуцирующими веществами. Главным недостатком данных методов является субъективность в определении конца титрования, а также необходимость в заместительном титровании, что повышает трудоемкость метода, а также значительно сказывается на погрешности измерения [ГОСТ 5903-89. Изделия кондитерские. Методы определения сахара. - С.131-141].
Аналогом изобретения является фотоколориметрический метод, основанный на обесцвечивании раствора гексацианоферрата (феррицианида) (III) калия в ходе реакции с редуцирующими веществами. О количестве редуцирующих веществ судят по остатку феррицианида после проведения реакции. Остаток феррицианида определяют по оптической плотности в кюветах с толщиной слоя 10 мм и со светофильтром, имеющим длину волны 440 нм относительно холостой пробы [ГОСТ 5903-89. Изделия кондитерские. Методы определения сахара. - С.144-147].
К недостаткам данного способа можно отнести:
1) использование феррицианида калия для окисления редуцирующих веществ, который по сравнению с раствором Фелинга значительно окисляет сахарозу;
2) при кипячении раствора происходит его концентрирование за счет интенсивного испарения влаги, в результате чего возникает повышение оптической плотности, вызывающее несистематическую погрешность параллельных опытов (невозможно добиться одинаковых быстроты нагрева, интенсивности кипения, быстроты остывания);
3) градуировочный график не подчиняется закону Бугера-Ламберта-Бера, поэтому данный метод не может гарантировать достоверного результата - рис.1.
Наиболее близким аналогом (прототипом) является способ, основанный на фотоколориметрировании медно-щелочного раствора (раствор Фелинга) после реакции с редуцирующими веществами. В пробирку вносят раствор сульфата меди, щелочной раствор сегнетовой соли, раствор желтой кровяной соли и исследуемый раствор. После пробирку нагревают на кипящей водяной бане в течение 3 минут, по истечении которых смесь фотометрируют на фотоколориметре при 670 нм относительно дистиллированной воды в кюветах с толщиной рабочего слоя 1 см. Параллельно проводят холостой опыт без нагревания. Содержание редуцирующих веществ определяют по уравнению для калибровочного графика .
Недостатками данного способа являются:
1) при выдерживании раствора на кипящей водяной бане происходит изменение его концентрации за счет интенсивного испарения влаги, в результате чего возникает повышение оптической плотности, вызывающее несистематическую погрешность измерений;
2) отсутствие поправки на частичное окисление нередуцирующих углеводов (например, сахарозы) реактивом Фелинга - рис.2, что крайне необходимо учитывать при анализе кондитерских изделий;
3) недостаточное время выдерживания на кипящей водяной бане - 3 минуты: за это время редуцирующие вещества не успевают прореагировать полностью, происходит изменение оптической плотности, что также вносит погрешность в определение - рис.3.
Техническим результатом предлагаемого способа является повышение точности и воспроизводимости анализа.
Технический результат достигается тем, что окисление редуцирующих веществ соединениями меди (II) в щелочной среде при нагревании на кипящей водяной бане в течение 10 минут, доведение объема охлажденного раствора до определенного значения, определение оптической плотности при длине волны 670 нм, введение поправки на частичное окисление нередуцирующих углеводов, которую вычитают из показания оптической плотности, и оценку концентрации редуцирующих веществ по калибровочному графику.
Сущность предлагаемого способа заключается в следующем.
Реактивы: раствор I: 34,66 г CuSO 4 ·5H 2 O в 1 л раствора; раствор II: 70 г NaOH, 173 г сегнетовой соли (калий натрий виннокислый) и 4 г желтой кровяной соли г в 1 л. Возможно приготовление раствора II без желтой кровяной соли, в этом случае необходима фильтрация или центрифугирование перед снятием оптической плотности исследуемого раствора.
Методика эксперимента
В мерную колбу вместимостью 25 мл вносят пипеткой по 5 мл растворов I и II и исследуемый раствор до 10 мл (стандартный раствор редуцирующего сахара), выдерживают 10 мин на кипящей водяной бане, охлаждают до комнатной температуры и доводят до метки дистиллированной водой, перемешивают (центрифугируют/фильтруют) и снимают показания оптической плотности при 670 нм относительно холостой пробы (по 5 мл растворов I и II, объем доведен до 25 мл), используя кювету шириной 10 мм. Значение оптической плотности берут по модулю.
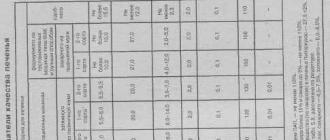
В случае если в исследуемом растворе содержатся нередуцирующие углеводы, например сахарозу (условно можно рассчитать как разность между общим сахаром и редуцирующими веществами) в значительных количествах, делают поправку по таблице.
Поправка на нередуцирующие углеводы при определении содержания редуцирующих веществ
Процентное содержание редуцирующих веществ в изделии находят по формуле:
где М - масса навески изделия, г; V - объем мерной колбы, в которой растворена навеска, мл; ν - объем раствора, взятый для анализа, мл.
1 г карамели (образец 1) растворяют в мерной колбе на 100 мл. В мерные колбы на 25 мл вносят реактивы и исследуемый раствор: 4, 6 и 8 мл, что соответствует 40, 60 и 80 мг изделия. Принимая влажность карамели 3% и содержание нередуцирующих углеводов 80% от сухого вещества, необходимо сделать поправку по табл. на показание оптической плотности во 2-ом случае на 0,005 и в 3-ем на 0,010.
Результаты сведены в таблицу.
1 г карамели (образец 2) растворяют в мерной колбе на 100 мл. Далее, как Пример 1.
1 г карамели, приготовленной в лабораторных условиях увариванием сахарного сиропа с патокой 1:1 до температуры 140°C, растворяют в мерной колбе на 100 мл. В мерные колбы на 25 мл вносят реактивы и исследуемый раствор: 2, 4, 6, 8 и 10 мл, что соответствует 20, 40, 60, 80 и 100 мг изделия. Для 3 определения принимаем поправку 0,005, для 4 - 0,010, для 5 - 0,020.
1 г патоки растворяют в мерной колбе на 100 мл. В мерные колбы на 25 мл вносят реактивы и исследуемый раствор: 2, 4, 5 и 6 мл, что соответствует 20, 40, 50 и 60 мг изделия. Принимая влажность патоки 22% и содержание нередуцирующих углеводов 70% от сухих веществ, поправку ни в одном случае делать не нужно (60*0,78*0,7<40).
Анализ хлеба на общий сахар. После кислотного гидролиза и нейтрализации водной вытяжки 6 г навески хлеба раствор доводят до 100 мл. В мерные колбы на 25 мл вносят реактивы и исследуемый раствор: 2, 4, 6 и 8 мл, что соответствует 120, 240, 360 и 480 мг изделия. Поправку вносить не нужно.
Предлагаемый способ отличается очень высокой воспроизводимостью и точностью по сравнению с аналогами.
Способ анализа редуцирующих веществ в сахаросодержащих средах, включающий окисление редуцирующих веществ соединениями меди (II) в щелочной среде при нагревании на кипящей водяной бане в течение 10 мин, доведение объема охлажденного раствора до определенного значения, определение оптической плотности при длине волны 670 нм, введение поправки на частичное окисление нередуцирующих углеводов, которую вычитают из показания оптической плотности, и оценка концентрации редуцирующих веществ по калибровочному графику.